- O nas
-
Branże
Branże
-
Edukacja, usługi, narzędzia
Edukacja, usługi, narzędzia
- Standardy i rozwiązania
-
Programy współpracy
Programy współpracy
- Kontakt
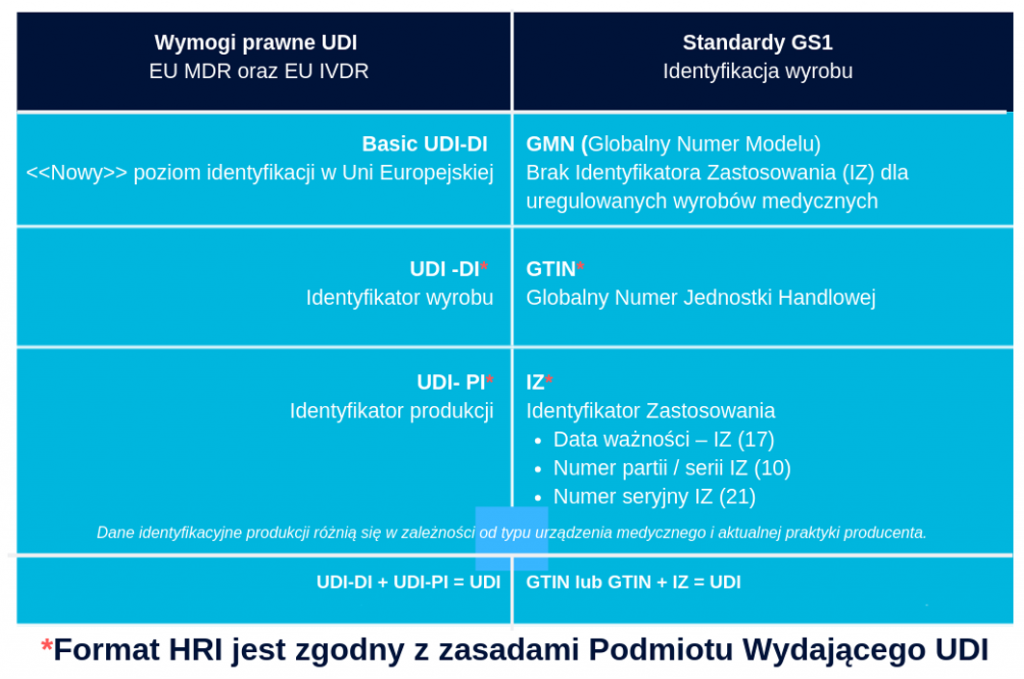
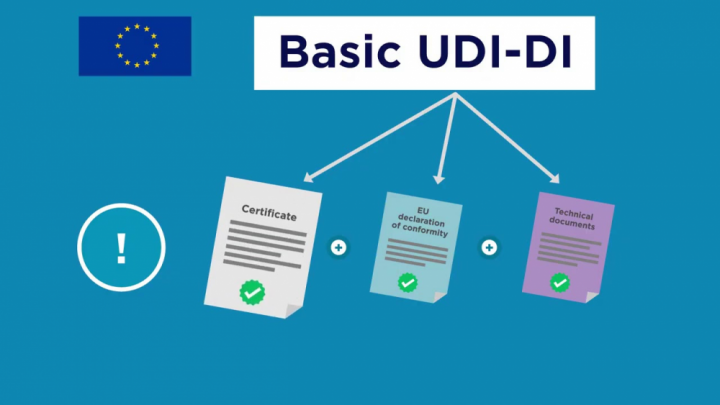
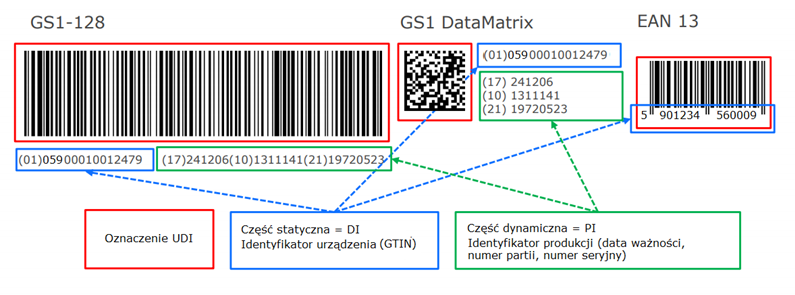
Co to jest UDI?
Unikalna Identyfikacja Wyrobów Medycznych (UDI) to system służący do oznaczania i identyfikacji urządzeń medycznych w łańcuchu dostaw opieki zdrowotnej w wymiarze globalnym.