- O nas
-
Branże
Branże
-
Edukacja, usługi, narzędzia
Edukacja, usługi, narzędzia
- Standardy i rozwiązania
-
Programy współpracy
Programy współpracy
- Kontakt
Dyrektywa fałszywkowa
Od 9 lutego 2019 roku – zgodnie z rozporządzeniem delegowanym do tzw. dyrektywy fałszywkowej (Dyrektywa Parlamentu Europejskiego i Rady 2011/62/UE z dnia 8 czerwca 2011 r.) leki wydawane na receptę (z wyłączeniem substancji, znajdujących się na tzw. białej liście) podlegają obowiązkowej serializacji. Jednym z jej elementów jest wprowadzenie na opakowanie leku tzw. niepowtarzalnego identyfikatora, który składa się z: kodu produktu, numeru seryjnego, daty ważności oraz numeru partii produkcyjnej.
Kod produktu, to identyfikator GTIN – numer od lat stosowany do identyfikacji produktów leczniczych w Polsce. Wszystkie dane wymagane dla leków wydawanych na receptę muszą być przedstawione w postaci dwuwymiarowego kodu kreskowego GS1 DataMatrix. Produkty OTC (z wyłączeniem leków, znajdujących się na tzw. czarnej liście) znakowane są w dotychczasowy sposób, z wykorzystaniem kodu kreskowego EAN-13.
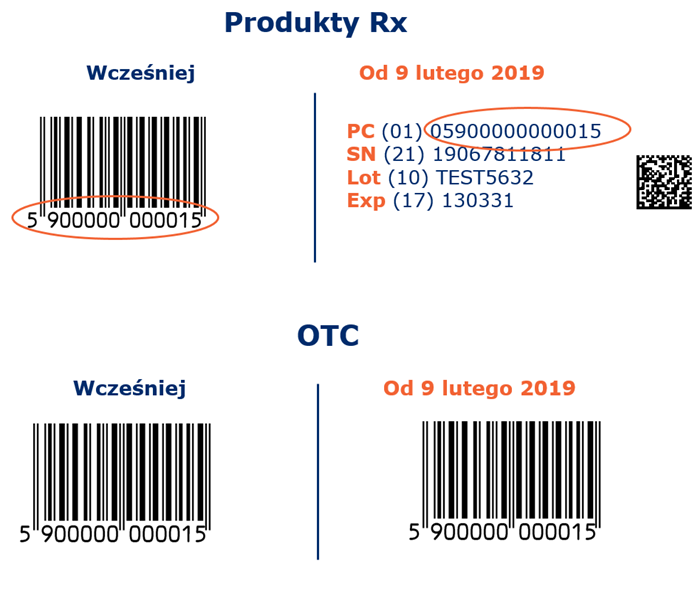
Komunikat Prezesa z dnia 7 lutego 2019 roku w sprawie zmiany kodów dla produktów leczniczych odnosi się do zmian, wynikających z tzw. obowiązku serializacji. W praktyce zmiana oznacza, że numery nadane przez Urząd zostaną poprzedzone nieznaczącym zerem w związku ze zmianą symboliki z kodu EAN-13 na kod GS1 DataMatrix. Nieznaczące zero nie zmienia struktury dotychczasowych 13-cyfrowych numerów GTIN. Numery nadane z puli Urzędu spełniają kryteria tzw. kodu produktu.





